Bimetallkorrosion oder Kontaktkorrosion?
Die Bimetallkorrosion, bekannt als Kontaktkorrosion, ist eine weitere Korrosionsart, die gemäß der DIN EN ISO 8044 auftritt, wenn zwei unterschiedliche metallische Werkstoffe in Kontakt stehen und einem Elektrolyten ausgesetzt sind. Beide Begriffe bezeichnen einen Korrosionsmechanismus, dessen elektrochemischen Reaktionen zwischen Metallen, die stark unterschiedliche Potentiale in der elektrochemischen Spannungsreihe aufweisen, resultieren.
Mechanismus der Bimetallkorrosion
Der Mechanismus der Bimetallkorrosion ist der einer galvanischen Korrosion, bei der die Anode und Kathode aus unterschiedlichen Metallen bestehen. Meist sind die Metalle separate Bauteile, sind aber über einen Elektrolyten oder durch andere metallische Bauteile kurzgeschlossen und bilden daher ein Korrosionselement. Die Kontaktkorrosion basiert, wie bei der galvanischen Korrosion, auch auf der elektrochemischen Spannungsreihe, die die Tendenz verschiedener Metalle und Legierungen zur Oxidation - also zum Elektronenverlust - beschreibt. Wenn zwei unterschiedliche Metalle, die in der Spannungsreihe weit auseinanderliegen, in Kontakt kommen und ein Elektrolyt vorhanden ist, entsteht ein galvanisches Element. Das Metall mit dem niedrigeren (unedleren) Potential wird zur Anode, während das edlere Metall zur Kathode wird. Dieser elektrochemische Unterschied fördert den Elektronenfluss von der Anode zur Kathode. Aus diesem galvanischen Element wird ein Korrosionselement, wenn das edlere und das unedlere Metall elektrisch Leitend verbunden werden. Wenn eine verkupferte Schraube oder auch nur ein Erdungskabel an ein Aluminiumgehäuse geschraubt wird, ist die Schraube die Kathode und das Aluminium die Anode (Bild 1), wodurch das Gehäuse schneller korrodiert. Umgekehrt ist eine verzinkte Schraube in einem Stahlgehäuse die Anode und korrodiert schneller (Bild 2).
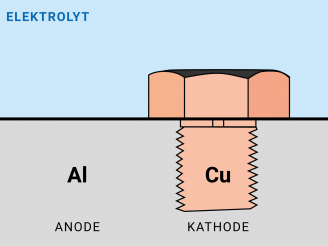
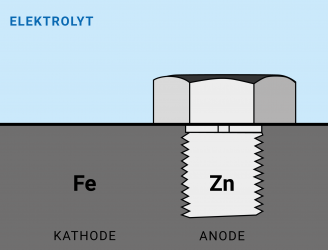
Die Korrosionsrate an der Anode wird nicht nur durch die Potentialdifferenz bestimmt, sondern auch durch die Stromdichte, die sich aus dem Verhältnis des tatsächlich fließenden Stroms zur Anode ergibt. Je größer die Fläche der Kathode im Vergleich zur Anode, desto geringer ist die Stromdichte und damit die Korrosionsrate an der Anode. Dies unterstreicht die Bedeutung der geometrischen Anordnung der beteiligten Metalle in der Praxis. Die Kontaktkorrosion Aluminium/Edelstahl oder die Kontaktkorrosion Aluminium/Kupfer wird daher nicht durch die Fläche des Kontaktes, z.B. einer Schraubverbindung, maßgeblich beeinflusst, sondern durch die Oberfläche und Potential der kombinierten Bauteile (Kontaktkorrosion Tabelle Link: Schraubenlexikon Korrosion, Arten, Ursachen, Schutz gegen Korrosion, Kontaktkorrosion (schrauben-lexikon.de)).
Verstärkung von Korrosionsarten durch die Kontaktkorrosion
Bimetallkorrosion teilt mehrere Mechanismen mit Oberflächenkorrosion und Spaltkorrosion, insbesondere die Rolle von Elektrolyten bei der Beschleunigung der Korrosionsreaktion. Die direkte Verbindung zwischen verschiedenen Metallen kann die Oberflächenkorrosion und auch einer Spaltkorrosion beschleunigen. Spannungsrisskorrosion ist ebenfalls relevant, da mechanische Spannungen durch die unterschiedlichen Ausdehnungskoeffizienten der Metalle verstärkt werden können.
Präventive Maßnahmen und Schutzstrategien gegen Kontaktkorrosion
Zur Vermeidung von Kontaktkorrosion ist passiver Korrosionsschutz eine effektive Methode. Durch die Anwendung von z.B. Korrosionsschutzwachsen oder anderen Beschichtungen wird eine physische Barriere geschaffen, die den direkten Kontakt zwischen den Metallen und den Elektrolyten verhindert. Dieser Ansatz verhindert die elektrochemische Reaktion, die Entstehung eines Stromflusses und damit die Korrosion. Für Bereiche mit starken Dehnungen und Schwingungen eignet sich besonders Korrosionsschutzwachs, das mit seinen selbstheilenden (selfhealing) Eigenschaften entstehende Risse und Verletzungen im Schutzfilm schließen kann.
Im Gegensatz dazu reduziert ein kathodischer Korrosionsschutz nur den Stromfluss, indem er die Potentialdifferenz zwischen den Metallen verringert. Dies wird häufig durch den Einsatz von Opferschichten aus Zinklegierungen erreicht, die ein niedrigeres Potential als das zu schützende Grundmaterial Stahl haben. Für größere Flächen werden auch Opferanoden oder Fremdstromanoden, die künstlich ein geringeres Potential aufrechterhalten, eingesetzt. Obwohl effektiv, verringert kathodischer Korrosionsschutz lediglich die Rate der Korrosion, anstatt sie vollständig zu unterbinden. Eine Kontaktkorrosion Aluminium/Kupfer z.B. durch eine Schraubverbindung eines Kupferkabels an einem Aluminiumgehäuse, lässt sich durch Korrosionsschutzwachs einfacher unterbinden als durch Opferanoden.
Zusammenfassung
Die Bimetallkorrosion ist ein kritischer Aspekt des Korrosionsschutzes, der tiefgreifendes Verständnis der Materialwechselwirkungen erfordert. Der passive Korrosionsschutz durch Beschichtungen bietet eine robuste Methode, um den direkten Kontakt mit Elektrolyt und Luftsauerstoff und damit den die elektrochemische Reaktion unterbindet, was zur vollständigen Verhinderung von Korrosionsreaktion führt.




